Dilution d'une solution
Nous avons vu dans l'article consacré à la préparation des milieux de culture qu'il était pratique de préparer des solutions concentrées appelées solutions mères, qui vont nous servir à préparer nos milieux de culture (solutions filles).
C'est aussi le cas lorsque l'on prépare la solution de microéléments rentrant dans la composition du milieu de Murashige et Skoog.
Certains quantités de composés chimiques comme celle du sulfate de cuivre CuSO4,5H2O (0,025mg.L-1) sont impossibles à peser avec des balances abordables. Nous devrons donc procéder par des dilutions successives jusqu'à obtenir la quantité voulue.
Généralités
Aspect qualitatif
Dans la vie de tous les jours, faire une dilution correspond à préparer un verre de sirop de grenadine par exemple.
Au fur et à mesure que l'on rajoute l'eau dans le verre contenant le sirop, le mélange prend une coloration plus claire. Nous avons dilué le sirop de grenadine dans de l'eau.
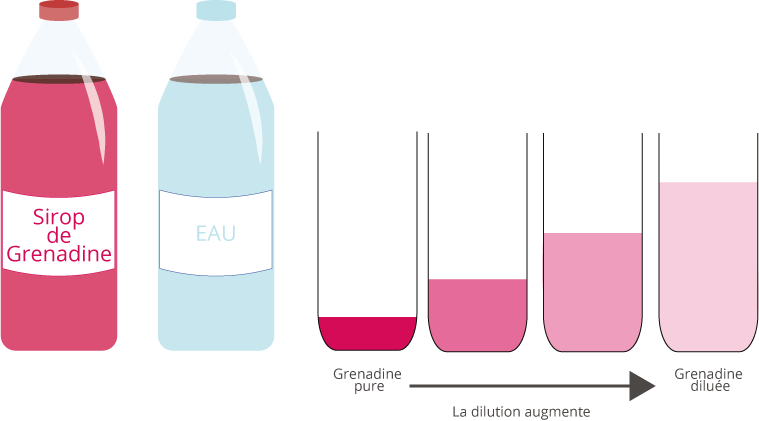
Pour le chimiste, la grenadine sera appelée le soluté et l'eau le solvant.
Aspect quantitatif
Pour reprendre l'exemple du sirop de grenadine, les fabricants de sirop nous donnent des conseils de dilution afin d'obtenir un goût agréable (et accessoirement nous alerter sur la valeur énergétique de la boisson!). Ici, 1 + 7 veut dire qu'il faut 1 volume de sirop pour 7 volumes d'eau.

Remarque: Pour les solutions que l'on utilise très régulièrement, il est plus simple de graduer un récipient en parts égales et d'ajouter le soluté et le solvant. C'est ce que je fais pour la préparation d'une solution désinfectante à l'Eau de Javel.
La concentration d'une solution
Pour savoir ce qui se passe au niveau des molécules qui constituent les solutions utilisées en culture in vitro, nous devons aborder la notion de concentration.
La concentration molaire Cm
C'est le nombre de mole par volume de solution. Elle est toujours exprimée par rapport à 1 litre de solution.

Quelque soit le volume, la concentration molaire est exprimée en mol/L.
De même, si je prélève 500 mL, 250 mL ou n'importe quel volume d'une solution 8 mol.L-1, la concentration molaire de cet échantillon sera toujours égale à 8 mol.L-1.

Autres façons d'exprimer la concentration
La concentration massique

Le pourcentage en masse

La molarité

Loi des concentrations
La molarité d'une solution mère (C1) multipliée par son volume (V1) est égale à la molarité d'une solution fille (C2) que multiplie son volume (V2).
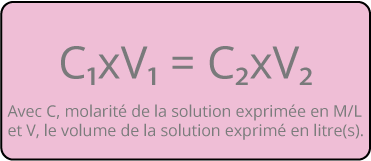

Glossaire
mole
La mole est une unité qui mesure un nombre d'objets extrêmement petits et nombreux, comme les molécules, les atomes, les électrons, les photons...
Un échantillon de matière de taille macroscopique contient un très grand nombre d'atomes.
Par exemple, 6 grammes d'aluminium contiennent environ 1,34×1023 atomes (134 000 000 000 000 000 000 000 atomes ; soit 134 000 milliards de milliards).
Pour éviter l'utilisation d'aussi grands nombres, on a créé une unité de mesure, la mole (dans le cas présent, 6 grammes d'aluminium représentent 0,22 mole d'atomes).
Une mole d’atomes contient environ 6,02214040×1023 atomes.
Ce nombre est appelé nombre d'Avogadro. Il est constant quel que soit l'élément quantifié. Autrement dit, de la même manière qu'il y a autant d'éléments dans une douzaine de pommes que dans une douzaine d'œufs, il y a le même nombre d'atomes dans une mole de carbone que dans une mole de plomb (soit 602 214 milliards de milliards d'atomes).
soluté
Espèce chimique introduite dans un solvant. Le soluté est par définition toujours en quantité moins importante que le solvant.
Il peut être:
- solide (sucre, charbon actif...)
- liquide (du sirop de grenadine...)
- ou gazeux (dioxyde de carbone des sodas...).
Solvant
espèce chimique dans laquelle est dissoute le soluté. Il est par définition en quantité nettement plus importante que le soluté
On utilise très souvent l'eau comme solvant.
Remarque: Certaines hormones sont dissoutes dans l'éthanol ou la soude molaire.
